-
jinnian金年会官网
- ACD/Labs
- Certara
- Labware / Sparta Systems
- Materials Design
- OmniComm System
- OPENTEXT
- QIAGEN
- UL
-
jinnianhui金年会官网
- 热线:021-32504385
- 微博:jinnian金年会官方网站入口
- 邮件:hzdongrun

2024-03-19 13:53:23 来源:jinnianhui金年会官网 作者:jinnian金年会官网
2018年8月25日下午,由中国药学会药物临床评价研究专业委员会主办、解放军总医院国家药物临床试验机构承办的《GCP实验室生物样本全链条标准化管理示范平台启动会暨GCP生物样本全链条标准化管理第二次学术沙龙》,在解放军总医院肿瘤大楼学术报告厅顺利召开。会场高朋满座,大咖云集,来自京内外临床试验机构、检测单位、申办方、CRO公司以及冷链运输单位等与生物样本链条密切相关的专家、同仁150余人齐聚一堂,共同分享各方在生物样本管理方面的经验与心得,并对GCP实验室生物样本的标准化管理展开了深入的探讨。

会议由中国药学会药物临床评价研究专业委员会主任委员王睿教授主持。王睿教授首先回顾了近年来国家出台的新政对药物研发领域的重大影响,特别指出“722事件”的警醒、一致性评价的要求,以及“重大新药创制科技重大专项”的重视,都对于药物临床评价特别是I期临床试验平台提出了更高的要求。

王睿教授还提到虽然GCP平台在信息化建设方面已有部分提升,但管理手段仍滞后于当今信息技术的发展,单位时间内多项目管理的能力仍有很大发掘空间。其中I期临床研究的核心要素“生物样本”,由于其存在样本数量大、信息核验与储运要求高等特点,对采集、分装、暂存、转运、检测直至最后储存的生物样本全链条管理提出了“高效、准确、快捷、智能”的更高标准。解放军总医院基于前期工作的经验,自主开发了“基于物联网的超低温智能样本管理系统”,并在实际工作中开展应用,且已在部分兄弟单位小范围推广。非常有幸的是,该系统于今年7月正式获得了北京市科委CRO平台的专项资助。
随后北京市科委生物医药处曹巍处长在大会致辞中强调,北京市科委对于药物研发行业的创新和发展非常重视,近年来已经持续资助了一批具有创新性和推动药物研发领域健康发展的项目。其中不少项目已经逐渐在行业中被广泛应用,帮助科研人员解决了不少工作中的实际问题,提高了新药研发领域的整体水平。今后北京市科委还将会持续对类似创新项目的进行支持,希望药物研发领域的科学技术水平始终保持强劲势头。

曹处长致辞之后,学术沙龙交流部分开始。首先由北京大学第一医院临床试验中心的赵侠教授就《临床生物样本质量管理及核查常见问题》作专题报告。赵侠教授介绍了北大第一医院临床试验中心I期临床试验研究室目前在生物样本管理方面的经验,并且分享了在实际工作中以及核查过程中经常遇到的典型问题。特别强调样本分装环节的重要性,以及错误分装给试验结果会带来严重的后果。同时提到,贴近I期临床实际工作的生物样本全流程的管理系统对于提高生物样本管理的正确性和高效性会有很大帮助。

在赵侠主任分享了生物样本管理及核查中的常见问题后,来自解放军307医院I期临床研究病房的田芳医师进行了《超低温物联网智能临床试验生物样本管理系统在GCP实验室的应用》的报告。作为解放军总医院的兄弟单位,解放军307医院I期病房年初安装由解放军总院I期试验室自主开发的“基于物联网的超低温智能样本管理系统”。田芳医师作为使用该系统的一线工作人员分享了使用心得。她指出,该样本管理系统在角色权限动态分配、消息机制、稽查痕迹、电子化文档管理、试验物品管理、工作流程分配等六个方面明显提升管理效率,与之前的纸质打印手工记录相比,系统应用后在人力资源得到极大节约,错误发生率有明显下降。

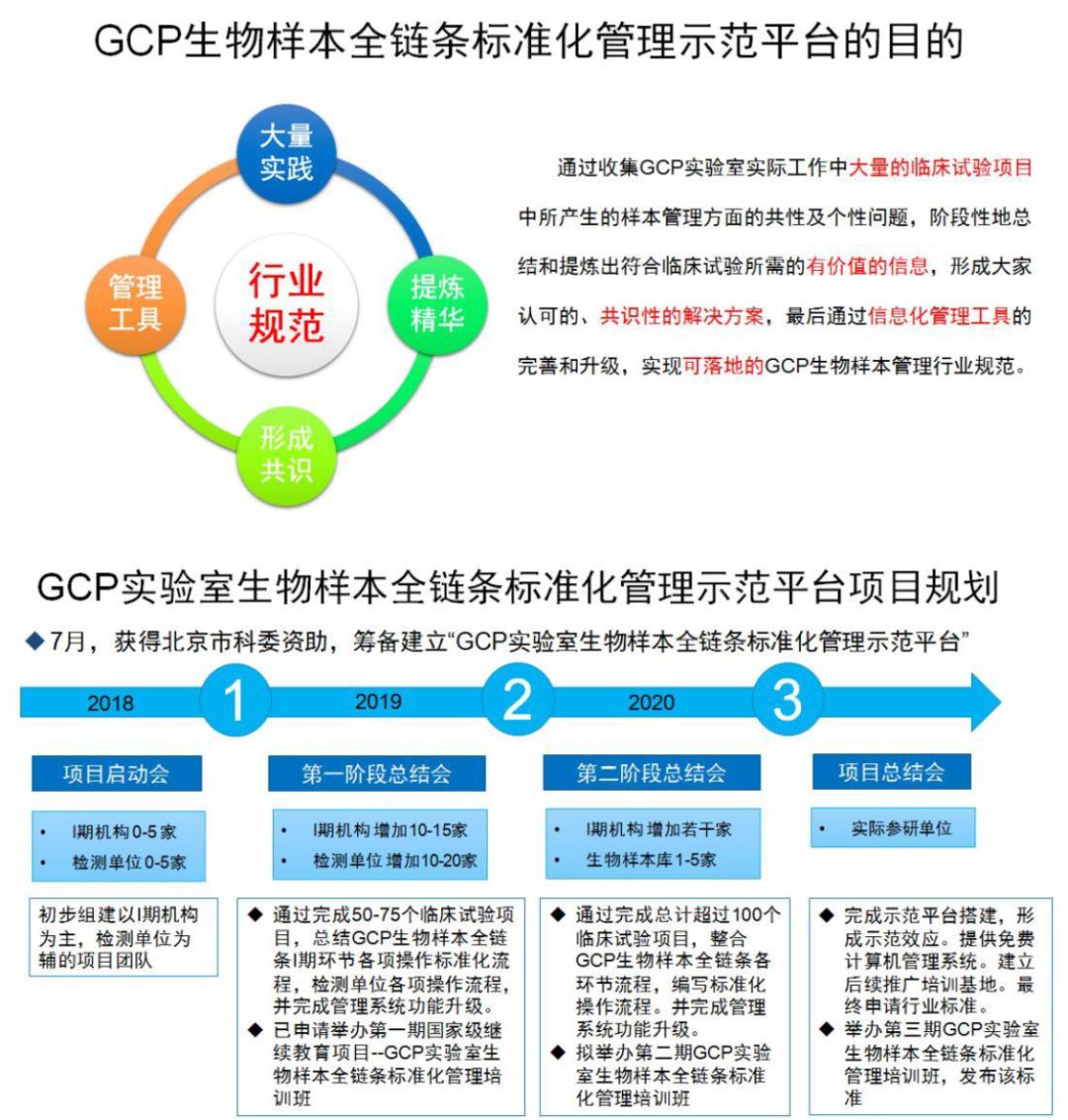
两个学术报告后,《GCP实验室生物样本全链条标准管理示范平台项目启动会》正式开始。由解放军总医院国家临床药物试验机构办公室主任王瑾教授向与会代表介绍“示范平台”项目的背景及规划。王瑾教授提到,解放军总医院药物临床研究中心遵循国家相关法规要求,结合自身实际工作场景,利用物联网技术手段,自主开发出一套适合GCP实验室生物样本管理流程的管理系统。首次打通临床机构与生物样本分析实验室之间的样本运送与接收链条,自动高效零差错接收并核验样本,减少样本间运输差错。同时首创样本管理系统多管分组核验流程,确保样品前处理分装流程零差错操作。该成果于今年6月通过北京市科委审评答辩,7月获得北京市科委CRO平台专项资助,用于建立“GCP实验室生物样本全链条标准化管理示范平台”。

“示范平台”项目规划通过收集GCP实验室实际工作中大量的临床试验项目中所产生的样本管理方面的共性及个性问题,阶段性地总结和提炼出符合临床试验所需的有价值的信息,形成大家认可的、共识性的解决方案,最后通过信息化管理工具的完善和升级,实现可落地的GCP生物样本管理行业规范。
启动会结束后,与会代表分为三批先后参观了解放军总医院I期试验病房,工作人员向参观代表实际演示了样本管理系统的工作流程。参观代表积极提问,现场交流气氛非常活跃。


当参观到样本分装核验环节时,大家对于样本分装“零差错”以及“三管核验架”的设计都给予了很高的评价。

参观结束后,来自20位入组单位专家进行了圆桌会议讨论,来自惠通医疗的袁松总经理作为该样本系统的技术支持单位,详细介绍了为本项目顺利实施提供人员和技术方面的保障的具体措施。

讨论环节,入组单位的专家们就今后“示范平台”建设纷纷发表了各自的建议,从项目命名到共识起草,从工作目标到任务分工都进行了充分深入的讨论。最终大家对今后项目组的工作方向形成了初步共识。
